高血压是全球最重要的公共卫生问题之一。据世界卫生组织(WHO)统计,全球超过 10 亿人患有高血压,每年导致超过 700 万人死亡。高血压是心肌梗死、脑卒中和终末期肾病的主要危险因素,对人类健康和社会经济造成沉重负担。尽管目前临床上已有多种药物用于降压治疗,如利尿剂、血管紧张素转换酶抑制剂(ACEI)、血管紧张素Ⅱ受体拮抗剂(ARB)、钙通道阻滞剂和β受体阻滞剂等,但这些药物普遍存在疗效有限、副作用明显以及耐药性等问题。在过去几十年间,医药界一直缺乏真正突破性的全新靶点用于新型高血压治疗药物的研发。
正常血压调控机制极为复杂。近年来越来越多的研究表明,氨基酸代谢失衡在高血压的发生和发展中发挥重要作用。然而,氨基酸必须依赖特异性转运蛋白进入细胞才能发挥作用,目前相关研究主要集中在少数氨基酸(如精氨酸)及个别转运体(如 SLC7A1)上。大量证据表明血管内皮细胞在血压稳态调节中发挥重要作用,但绝大多数氨基酸转运体在血管内皮细胞的表达调控及在血压调节中的作用仍所知甚少。因此,全面揭示氨基酸及其转运系统对血压稳态的影响,对于理解高血压发生机制以及开发新型干预策略具有重要意义。
2025年9月3日,华东师范大学医学与健康研究院张晓燕教授、管又飞教授联合华中科技大学同济医院汪道文教授团队,在国际权威期刊《Science Translational Medicine》 发表了题为 “Inhibiting SLC38A2 lowers blood pressure in rodent models of hypertension” 的研究论文。该研究首次揭示了血管内皮氨基酸转运体 SLC38A2 在血压调控中的关键作用及分子机制,并因其突出的创新性及重要性被期刊选为当期封面亮点(Featured Cover Image)。

张晓燕教授研究团队利用转录组学分析发现,SLC38A2 在人脐静脉内皮细胞(HUVECs)中高水平表达,并在高盐饮食诱导的盐敏感性高血压大鼠主动脉内皮细胞中显著上调(图1)。
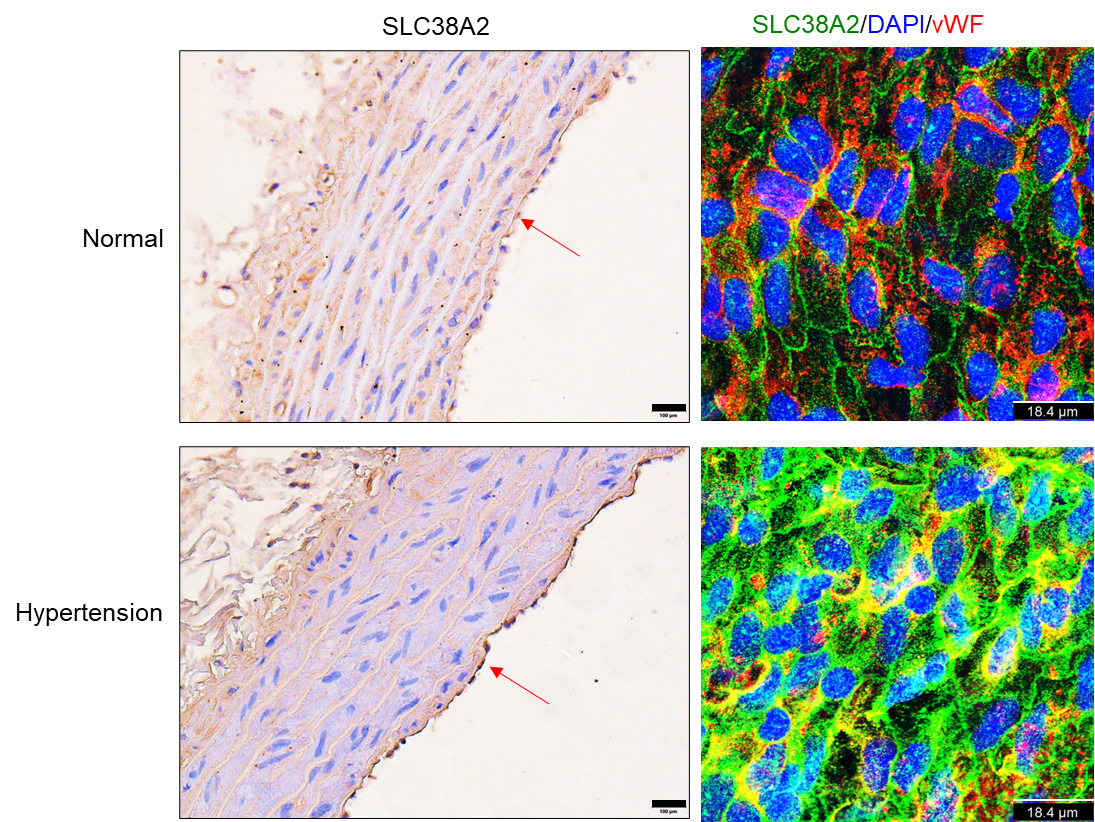 |
图1. SLC38A2在高盐饮食诱导的盐敏感性高血压大鼠主动脉内皮细胞中表达显著上调。
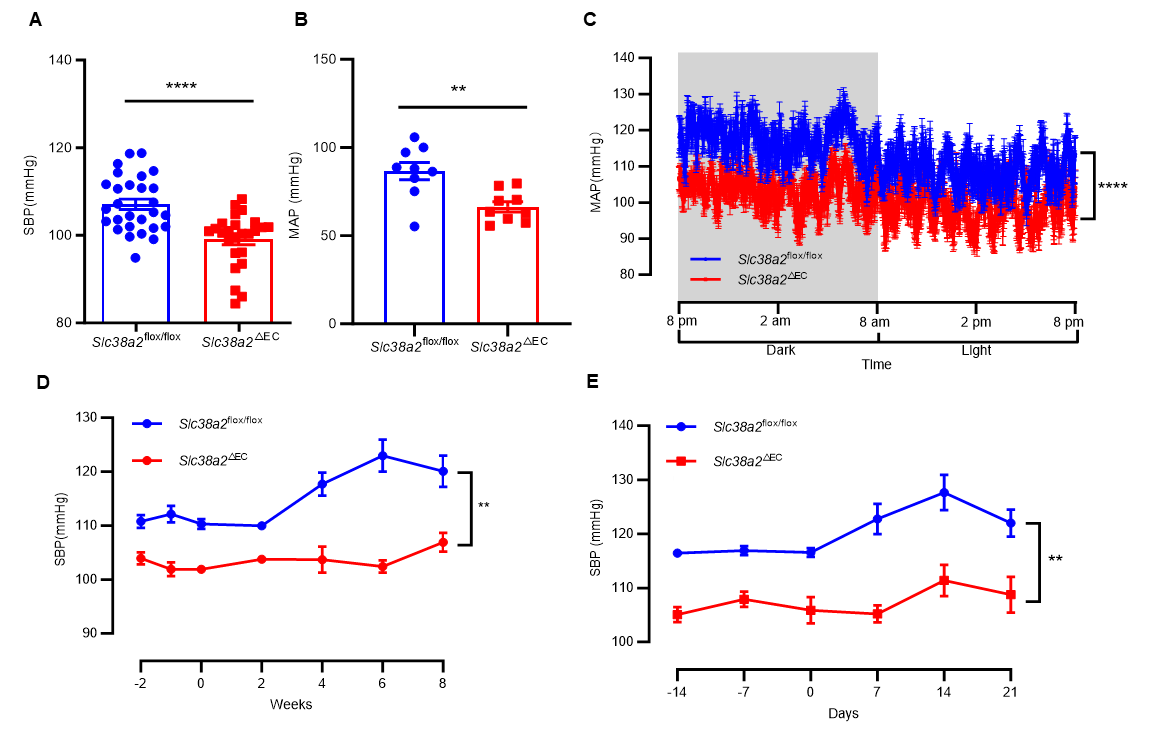
为了深入探究SLC38A2在血管内皮功能中的具体作用,该研究团队构建了内皮细胞特异性Slc38a2基因敲除小鼠(Slc38a2△EC)。研究发现,与对照组相比,Slc38a2△EC小鼠的基础血压显著降低,并对高盐饮食及DOCA盐处理所诱发的高血压表现出明显的抵抗能力(图2)。该研究首次在功能层面上揭示了血管内皮细胞中SLC38A2的关键作用,证实其缺失不仅可降低基础血压,还能延缓高血压的进展。
|
图2. Slc38a2△EC 小鼠基础血降低(A-C),并能抵抗高盐(D)和 DOCA 盐(E)诱导的高血压。
为了阐明内皮细胞SLC38A2缺陷抵抗高血压的机制,研究团队使用单细胞转录组测序(scRNA-seq)技术评估了小鼠主动脉各细胞亚群的mRNA表达谱,结果显示Slc38a2△EC小鼠动脉内皮细胞中一氧化氮(NO)合成通路相关基因显著上调,而血管平滑肌细胞中的 cGMP-PKG 信号通路也被明显激活。进一步的研究发现,内皮细胞SLC38A2 的缺失导致细胞内谷氨酰胺水平的明显降低,继而激活 AKT-eNOS 信号通路、显著增加 NO 的生成,进而促进血管舒张并降低血压(图3)。
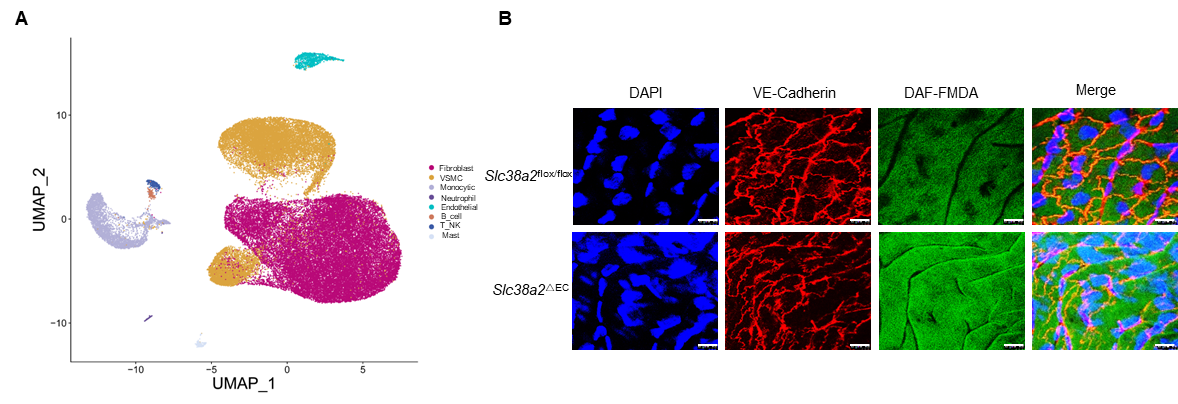 |
图3. 单细胞测序(A)显示Slc38a2△EC 小鼠动脉内皮细胞NO 合成通路显著活化,导致主动脉内皮细胞NO水平的显著增高(B)。
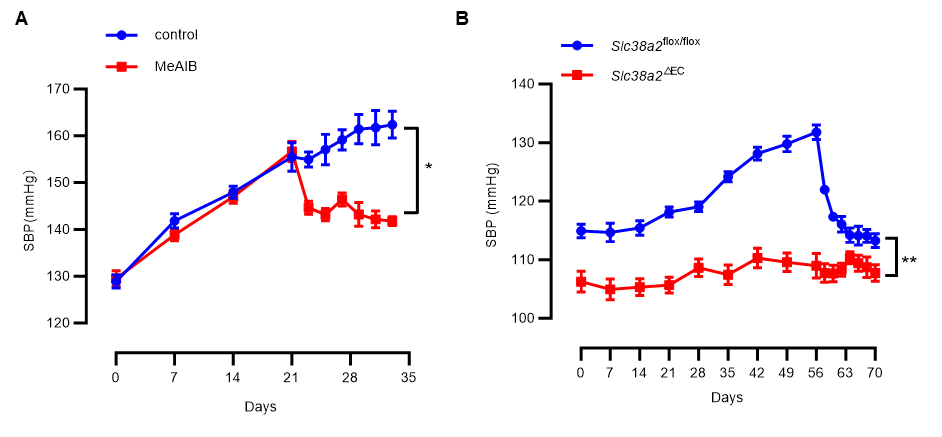
研究团队进一步发现,SLC38A2 的小分子竞争性抑制剂 MeAIB 在动物模型中也展现出显著的降压效果。MeAIB 干预不仅降低了小鼠的基础血压,还能有效减轻高盐饮食诱导的小鼠高血压以及盐敏感 Dahl-SS 大鼠的血压升高,同时显著改善血管舒张反应(图4)。这一发现为靶向SLC38A2的药物干预策略提供了坚实的临床前依据,显示出该靶点具备良好的转化医学潜力。
|
图4. SLC38A2 竞争性抑制剂 MeAIB 显著降低高盐诱导的盐敏感Dahl-SS大鼠(A)和小鼠(B)的高血压。
为了进一步明确SLC38A2与人群高血压的相关性,团队对UK BioBank及华中高血压队列的遗传学数据进行了分析,发现 SLC38A2 基因位点 rs1873793 多态性与高血压发生风险密切相关,并在中国和欧洲两个队列人群中均得到验证。该结果进一步支持SLC38A2在高血压发生中的关键作用,提示其不仅在动物模型中对血压水平具有影响,也显示作为人群高血压预测标志物和干预靶点的潜在价值。
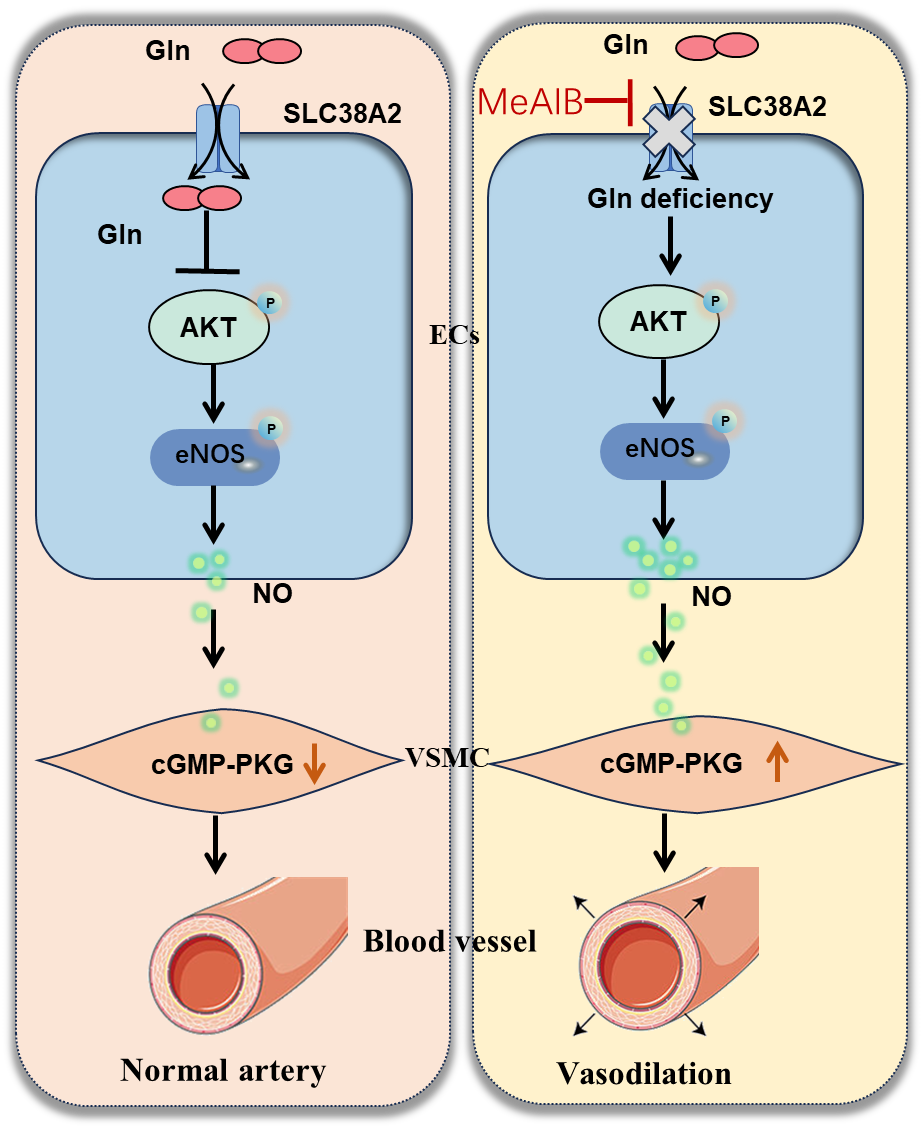
该研究通过整合分子机制探索、动物模型验证及人群遗传学证据,系统阐明了氨基酸转运体SLC38A2在血压调控中的核心功能。研究首次确立了氨基酸转运体与高血压发生和发展之间的直接联系,不仅深化了对高血压病理机制的理解,也为开发新型降压药物提供了极具前景的全新靶点,具有重要的科学意义和临床转化潜力(图5)。
|
图5. SLC38A2调控血压稳态的机制。
该工作是张晓燕教授关于中性氨基酸转运体SLC38A2与心肾稳态调控关系系列研究的最新成果,在前期的研究中张晓燕教授团队发现SLC38A2作为肾脏渗透压反应基因在维持肾脏髓质高渗梯度及肾脏尿液浓缩功能中的重要作用(Elife. 2023;12:e80647)。本研究中张晓燕教授、管又飞教授和汪道文教授共同担任通讯作者,华东师范大学杜春秀博士后和徐虎副教授共同担任第一作者。
上述研究得到了国家自然科学基金委优秀青年基金及面上基金项目的支持。
原文链接:http://doi.org/10.1126/scitranslmed.adt5947