肺动脉高压(PAH)是一种进行性发展的、危及生命的心血管疾病,其核心病理特征是肺部血管系统发生重塑,主要表现为缺氧微血管的过度收缩以及血管中层肺动脉平滑肌细胞(PASMCs)的异常增殖。这种重塑会导致肺血管阻力不断攀升,最终引发右心室衰竭。尽管目前的靶向药物(靶向内皮素、一氧化氮途径等)能通过促进血管扩张来缓解症状,但PAH依然具有极高的致命性,临床上迫切需要能够抑制平滑肌细胞增殖、从根本上逆转肺血管重塑的创新疗法。
近日,华东师范大学医学与健康研究院陈丽红教授联合上海健康医学院基础医学院杨光锐教授,在国际权威综合期刊《Nature Communications》(中科院一区,IF:15.7)上发表了题为“Targeting REV-ERBα/BNIP3 axis attenuates pulmonary arterial hypertension by repressing mitophagy in mice”的最新研究成果。该研究首次证实生物钟核受体REV-ERBα(尤其是血管平滑肌细胞来源的REV-ERBα)是遏制PAH病程进展的关键保护因子,并创新性揭示受REV-ERBα调控的线粒体自噬相关蛋白BNIP3在PAH中发挥关键致病作用。同时,研究进一步阐明了靶向REV-ERBα/BNIP3信号轴在PAH治疗中的潜在应用价值。

1.关键发现 研究团队首先发现,在SuHx诱导的小鼠肺动脉高压模型以及缺氧暴露的原代大鼠PASMCs中,生物钟核受体REV-ERBα的蛋白及mRNA表达水平均出现了特异性的显著下降。与之形成鲜明对比的是,同家族的REV-ERBβ表达并未发生改变。通过构建多种基因修饰小鼠模型,研究证实了敲除Rev-erbα基因(尤其是血管平滑肌细胞特异性敲除)会显著加剧SuHx诱导的PAH和肺血管重塑,而Rev-erbβ基因敲除则对PAH的表型没有任何影响。
2.机制突破 在探索具体机制时,研究人员发现REV-ERBα能够直接结合到非经典线粒体自噬受体基因Bnip3的启动子区域,并对其转录产生抑制作用。这种对Bnip3的抑制直接阻断了BNIP3驱动的异常线粒体自噬,从而在缺氧的PASMCs中维持了线粒体的稳态与功能。研究进一步表明,敲低Bnip3能够抑制缺氧诱导的细胞增殖,而过度表达Bnip3不仅会抵消REV-ERBα的保护作用,还会独立加速PAH的病理进程。
3.治疗验证 研究团队对靶向生物钟核受体REV-ERBα在PAH中的治疗潜力进行了验证。研究发现,小分子化合物SR9009,能够以REV-ERBα依赖的方式显著抑制缺氧诱导的PASMC增殖。在动物模型中,无论是在PAH疾病发展期给药,还是在PAH疾病晚期进行干预,SR9009均能能显著改善肺动脉高压、减轻肺血管增厚,并逆转已建立的右心室重塑。同时,通过腺相关病毒介导在体内过表达Rev-erbα,同样可显著缓解SuHx诱导的PAH及肺血管和右心重塑 。
4.研究意义与展望 该研究首次报道并系统阐明了生物钟核受体REV-ERBα和线粒体自噬相关蛋白BNIP3在PAH发生发展中的协同作用机制(图1)。靶向REV-ERBα/BNIP3这一“节律-线粒体”调控轴,不仅为阐释PAH的复杂病理机制开辟了新视角,也为基于生物钟靶向的心血管和代谢性疾病的防治奠定了理论基础,展现出重要的临床转化价值。
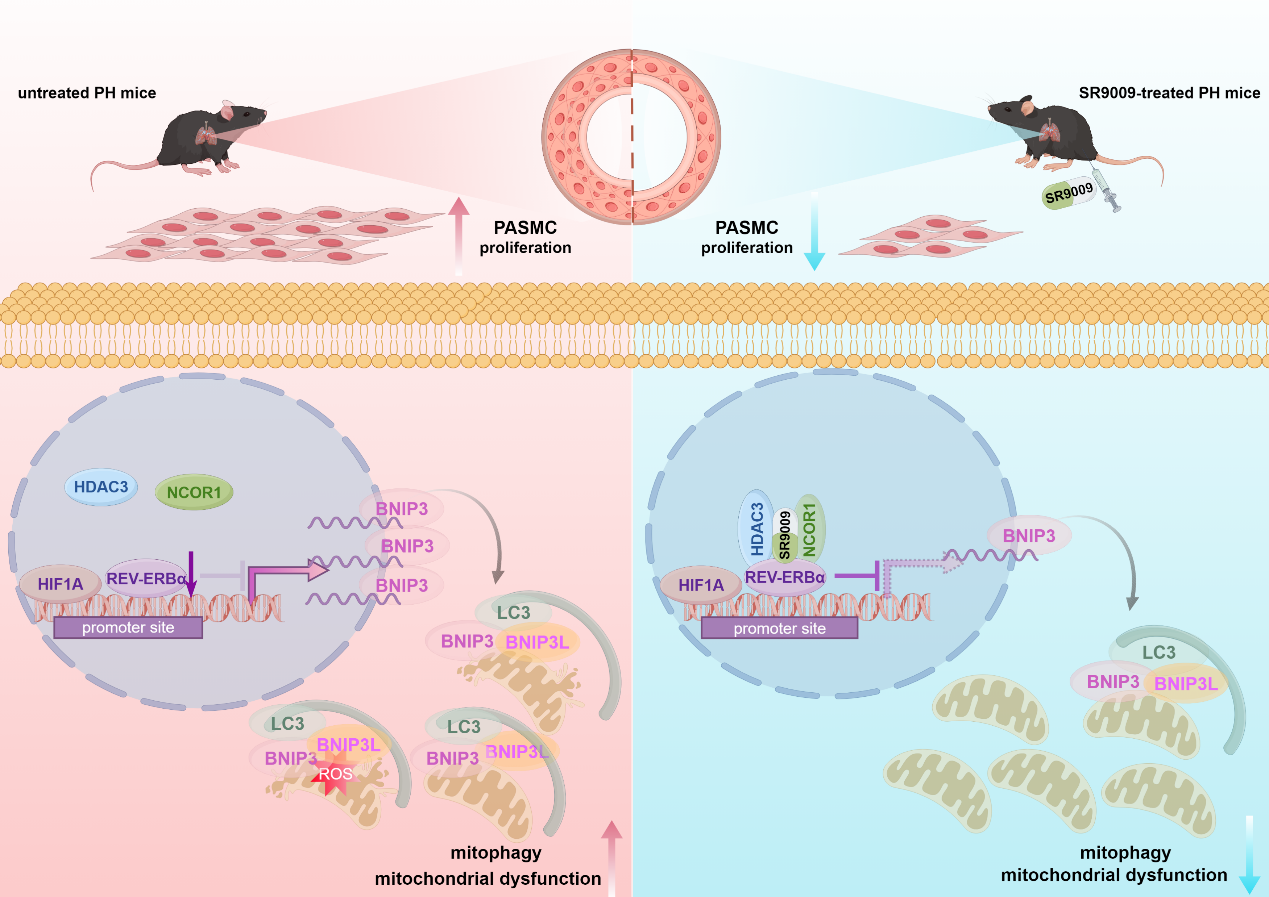
图1 REV-ERBα/BNIP3信号轴在肺动脉高压中的作用模式图。
该研究由华东师范大学医学与健康研究院陈丽红教授团队、上海健康医学院基础医学院杨光锐教授团队合作完成。研究得到了大连医科大学管又飞教授、华东师范大学张晓燕教授、郑丰教授、徐虎副教授,和西安交通大学第一附属医院范粉灵教授的大力支持。华东师范大学邱乐佳博士为文章的第一作者。研究得到了科技创新2030 -“四大慢病”国家科技重大专项和国家自然科学基金面上项目的基金支持。
原文链接:
https://doi.org/10.1038/s41467-026-71189-2
